이번 KOGO 학회의 1일차에서는 KAIST 최정균 교수님의 ‘Development and Clinical Validation of AI Models for Neoantigen Prediction‘ 세션을 들었습니다.
✔️ 우선 세션 내용을 살펴보기에 앞서, 이해를 돕기 위해 먼저 몇 가지 관련 개념을 짚고 넘어가겠습니다.
🧬 암 백신(Cancer vaccine)이란?
암 백신(Cancer vaccine)은 환자의 면역 시스템을 활용하여 암세포를 공격하도록 유도하는 치료법입니다.
우리 몸의 면역세포는 본래 🧬 항원(antigen)이라는 특정 신호를 인식해 비정상적인 세포를 구분하는데,
암 백신은 이 메커니즘을 활용해 암세포의 항원을 면역계에 학습시키는 치료법입니다.
🎯 암 백신 설계의 핵심 포인트
암 백신에서 가장 중요한 요소는 2가지 입니다.
- Target : 어떤 항원을 선택할 것인가?
- Delivery : 그 항원을 어떤 방식으로 면역 시스템에 전달할 것인가?
이에 따라 면역 반응의 강도(immunogenicity)와 특이성(specificity)이 달라지기 때문입니다.
🧐 어떤 항원이 좋은 Target일까?
모든 암에서 공통적으로 발견되는 항원을 target으로 사용할 수도 있지만, 이런 항원은 효과가 충분하지 않을 수 있습니다.
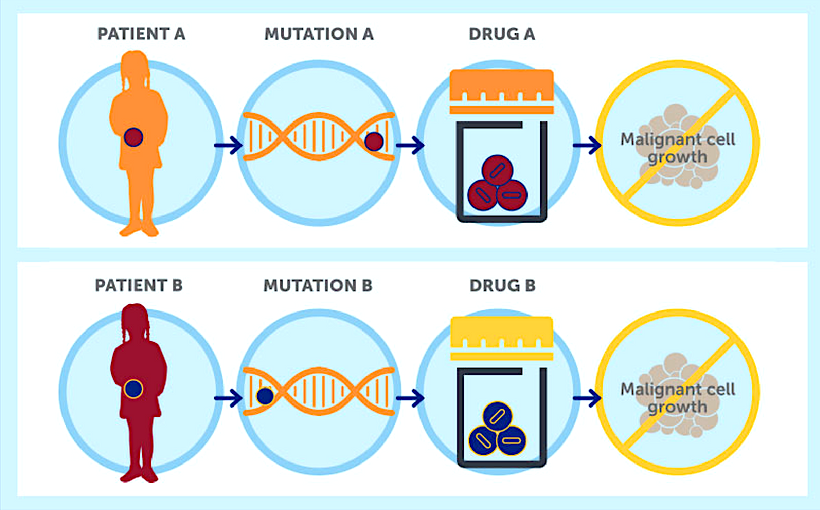
이에 따라 최근에는 환자마다 서로 다른 target을 기반으로 개발되는 개인 맞춤형(personalized) 암 백신이 주목받고 있습니다.
이는 환자의 유전체 정보와 종양 특성에 기반한 precision medicine(정밀의료)의 대표적인 사례로 볼 수 있습니다.
🧬 신항원(Neoantigen)이란?
이러한 개인 맞춤형 암 백신의 핵심 개념이 바로 neoantigen입니다.
암세포는 돌연변이로 인해 정상 세포에는 없는 새로운 단백질을 만들 수 있는데, 이러한 단백질을 🧬 neoantigen이라고 합니다.
Neoantigen은 ✅ 정상세포에는 없고 ✅ 암세포만 구분할 수 있어 비교적 특이적이고, 안전한 target으로 주목받고 있습니다.
🧬 Peptide-MHC(pMHC) 란?
개인 맞춤형 암 백신과 neoantigen을 이해하려면 먼저 peptide-MHC 개념을 알아야 합니다.
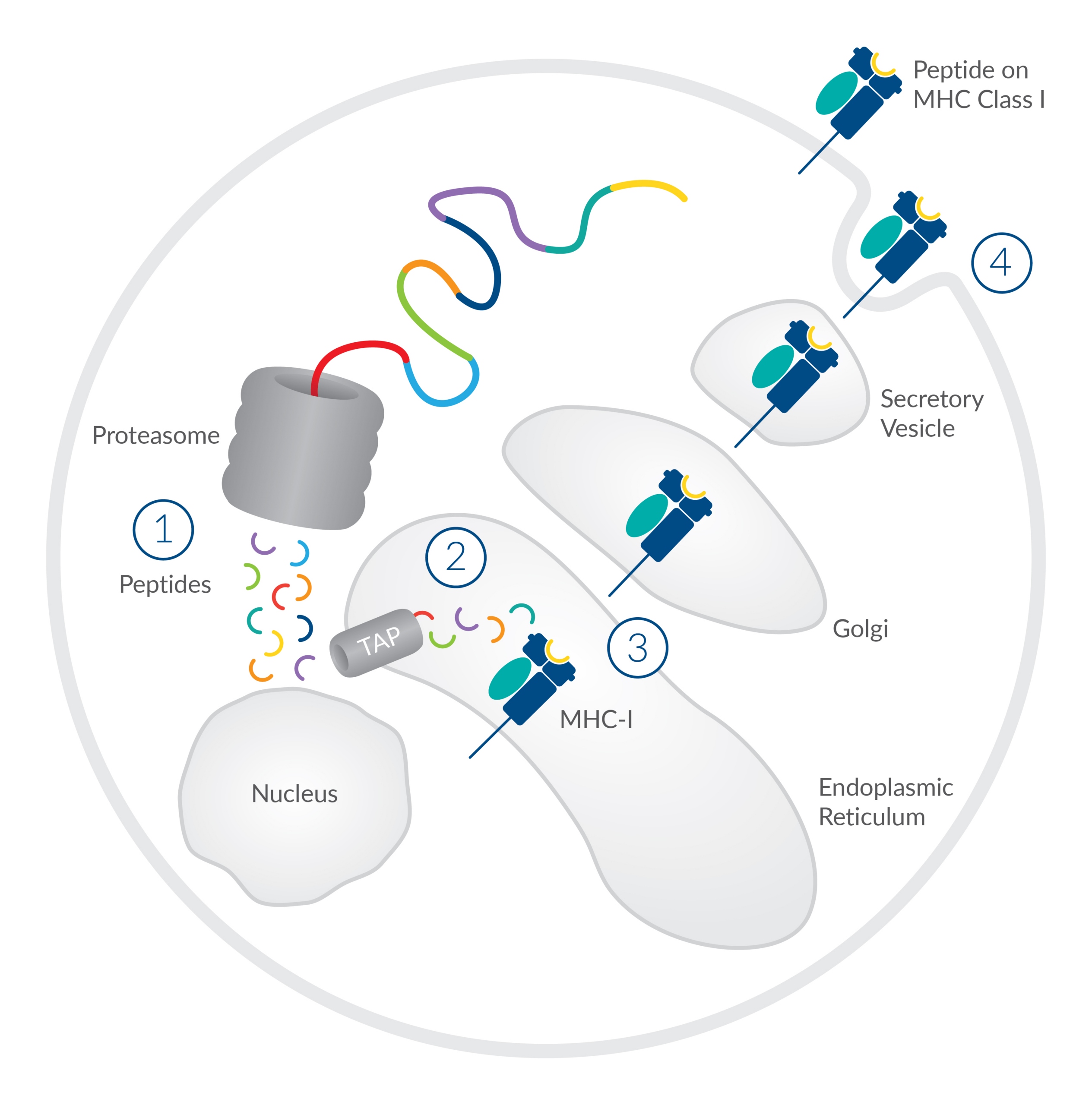
우리 몸의 세포 표면에는 🧬 MHC가 존재하는데, 이는 세포 내부의 단백질 조각(peptide)을 표면에 보여주는 역할을 합니다.
(아래 그림의 ③, ④ 참고)
👉🏻 즉, peptide-MHC(pMHC)는 peptide와 MHC가 결합된 형태로, 세포 상태를 면역계에 알리는 표지판🪧입니다.
MHC는 2종류의 Class (I과 II)가 있으며, 각각 다른 방식으로 peptide를 제시해 서로 다른 면역세포 반응을 유도합니다.
✔️ 이러한 개념을 이해한 상태에서, 이번 세션에서 다뤄진 내용을 살펴보겠습니다.
🧬 Personalized Cancer Vaccine
한 제약사의 2024년 발표에 따르면, 최근 바이오 R&D 영역에서도 단순한 실험뿐만 아니라
AI 분석과 대규모 컴퓨팅(compute at scale)이 필수적이라고 하였습니다.

바이오 R&D 분야에는 개인 맞춤형 암 백신(Personalized Cancer Vaccine) 개발도 포함됩니다.
이 연구의 핵심 중 하나는 종양에서 발견된 변이 중 실제로 면역 반응을 유도할 수 있는 neoantigen을 정확히 예측하는 것입니다.
대표적인 neoantigen 예측 연구로는 TESLA(Tumor Neoantigen Selection Alliance)가 있습니다.
논문에 따르면, 예측된 608개의 pMHC 후보 중 단 37개만이 실제로 T세포의 면역반응을 유도하는 것으로 확인되었습니다.
이는 🙁약 6%에 불과하며, 이에 대한 원인으로는
1. 이미 해당 antigen에 이미 저항성(immune tolerance)이 있거나
2. HLA Class II를 고려하지 못한 예측 한계의 가능성이 제시되었습니다.
📌 DeepNeo
이러한 한계를 보완하기 위해, 이번 세션의 연자가 개발한 AI 기반의 개인 맞춤형 암 백신 플랫폼이 바로 DeepNeo입니다.
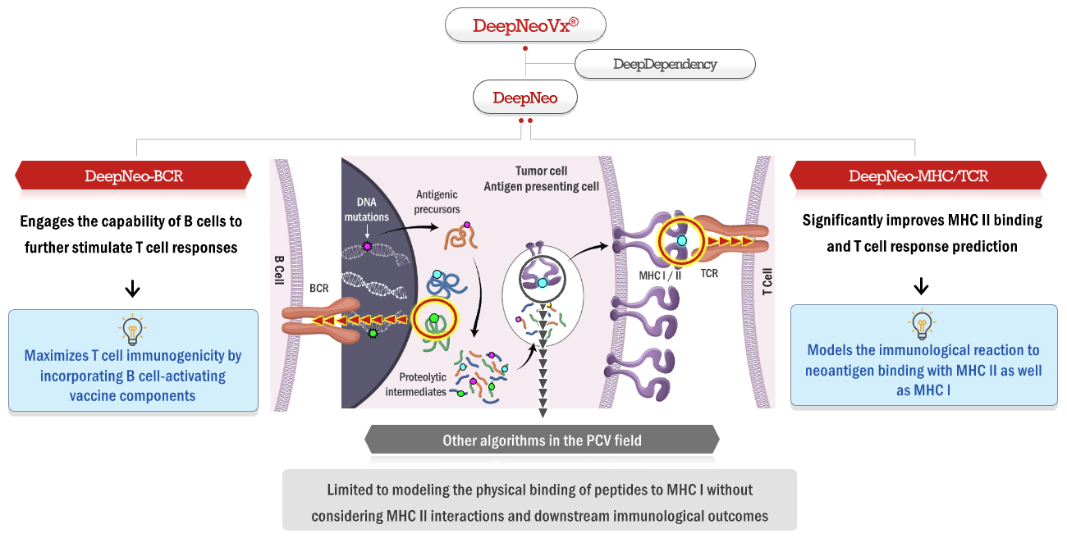
해당 플랫폼에는 총 3가지 AI 모델이 포함되어있습니다.
1. DeepNeo-MHC
▶ Peptide와 MHC의 binding을 예측
항원이 면역 반응을 일으키려면 먼저 MHC라는 단백질과 결합해야합니다.
해당 모델은 항원(peptide)이 MHC과 결합을 할 수 있는지 예측하는 모델입니다.
2. DeepNeo-TCR
▶ pMHC와 TCR의 인식 여부 예측 (immunogenecity)
MHC에 결합한 peptide가 실제 면역반응을 일으키려면 T세포의 수용체(TCR)가 이를 인식해야합니다.
해당 모델은 peptide-MHC 복합체를 TCR이 인식할 수 있는지 예측하는 모델입니다.
이를 통해 MHC Class I 뿐만 아니라 Class II에 대한 예측력도 향상시킬 수 있었다고 합니다.
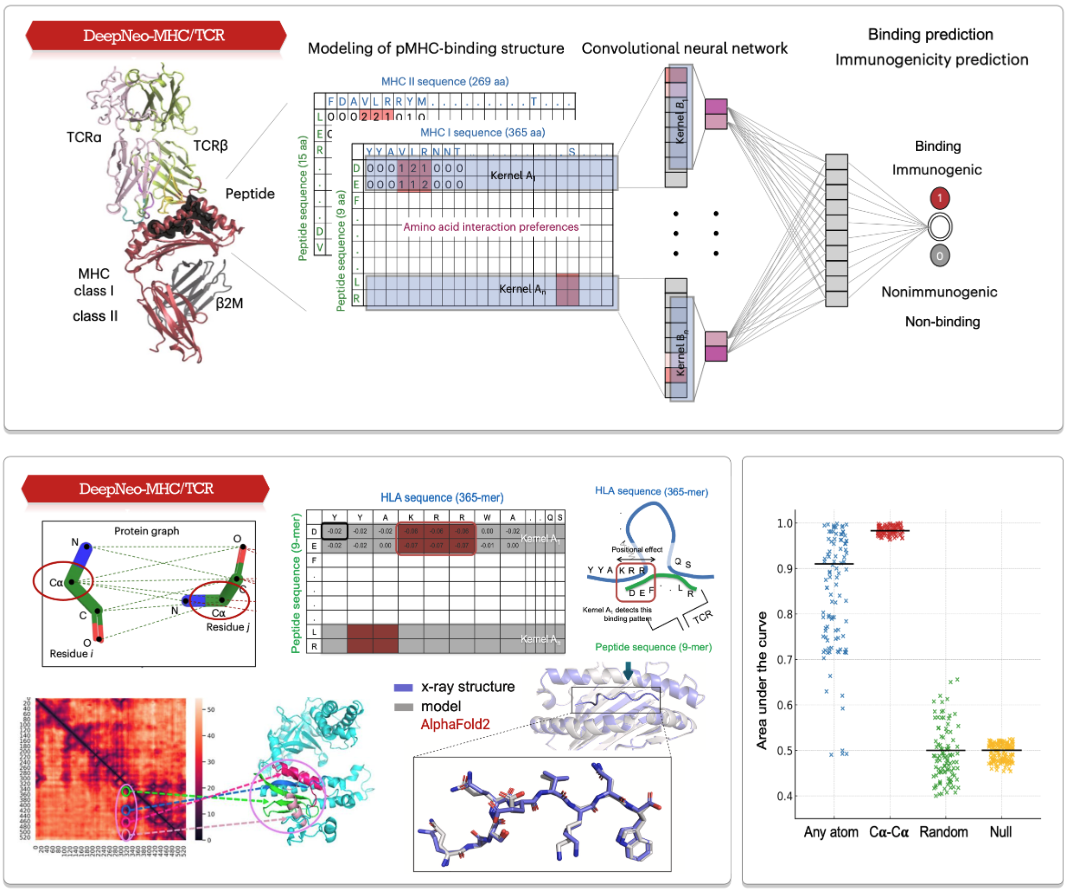
DeepNeo-MHC/TCR 모델은
peptide와 MHC 서열정보를 아미노산 간 상호작용 matrix 형태로 변환 후, CNN을 사용하여 패턴을 학습하도록 설계되었습니다.
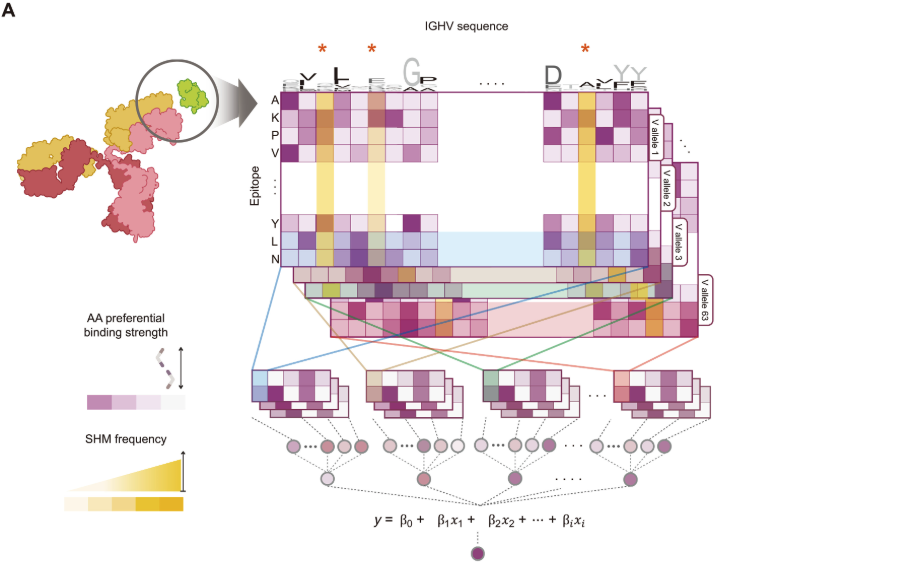
3. DeepNeo-BCR
▶ Neoantigen과 BCR의 결합 가능성 예측
항원이 B세포의 면역반응을 유도하려면 해당 항원을 B세포 수용체(BCR)와 결합할 수 있어야합니다.
즉, 기존 neoantigen 예측 방법에서 한 단계 더 나아가,
👉🏻 B세포가 해당 neoantigen을 실제로 인식할 수 있는지까지 평가하는 모델입니다.
해당 모델 또한 CNN 기법을 사용하여 만들어졌습니다. (그림 참고)
(언어 모델링도 도입을 했지만 CNN에 비해 성능이 좋지는 않았다고 합니다)
DeepNeo-BCR 모델의 경우, mouse 모델 뿐만 아니라 TCGA 및 임상 데이터를 활용해 validation을 진행하였는데,
👉🏻 TCGA 데이터에서는 BCR과 반응성이 높다고 예측된 neoantigen이 실제 면역 선택 신호와 연관됨이 확인되었고,
👉🏻 임상 환자 데이터에서는 해당 예측 점수가 면역반응 강도와 치료 반응 예측과도 유의미하게 연관됨이 보고되었습니다.
또한, 환자 내 여러 neoantigen 중 🧫 B세포 반응성이 높은 neoantigen이 포함된 경우,
환자의 T세포 면역반응(T cell activity)가 전반적으로 높아지는 경향이 관찰되었습니다.
이는 B세포가 neoantigen을 인식함으로써 면역 환경 전반에 긍정적인 영향을 미칠 수 있음을 시사합니다.
✏️ 마무리
이외에도 neoantigen cryptic peptide나 차세대 cancer model, 그리고 다양한 공동연구 사례들이 함께 소개되었습니다.
이러한 발표들은 AI 기반 neoantigen 예측 연구가 빠르게 확장📈되고 있음을 보여주었습니다.
특히 연구 범위가 알고리즘 개발을 넘어 실제 👩🏻🔬임상 검증 단계까지 이어지고 있다는 점이 인상적이었습니다.
이들 연구는 공통적으로 방대한 생물학 데이터 분석을 기반으로 이루어지며, 그 중심에는 🧬유전체 데이터가 있습니다.
이를 효과적으로 분석하기 위해서는 대규모 데이터 처리와 반복 연산🧮이 필수적이며, 곧 연구 수행의 핵심 기반이 됩니다.
따라서 이런 흐름은 확장 가능한 컴퓨팅 인프라가 바이오 AI 시대의 필수임을 보여주는 대표적인 사례라고 생각되었습니다.
이상 AI 기반 neoantigen 예측 연구의 현재와 가능성을 살펴본 세션 정리였습니다.
긴 글 읽어주셔서 감사드리며, 다음에 또 유익한 내용으로 찾아뵙겠습니다 ☺️
SA 서희재